近日,欧盟委员会公布最新一期的《MDR/IVDR认证和申请的公告机构调查结果》,为该项目启动以来的第8次调查,调查数据截止于2024年2月29日。
1.MDR申请提交与证书颁发的数量
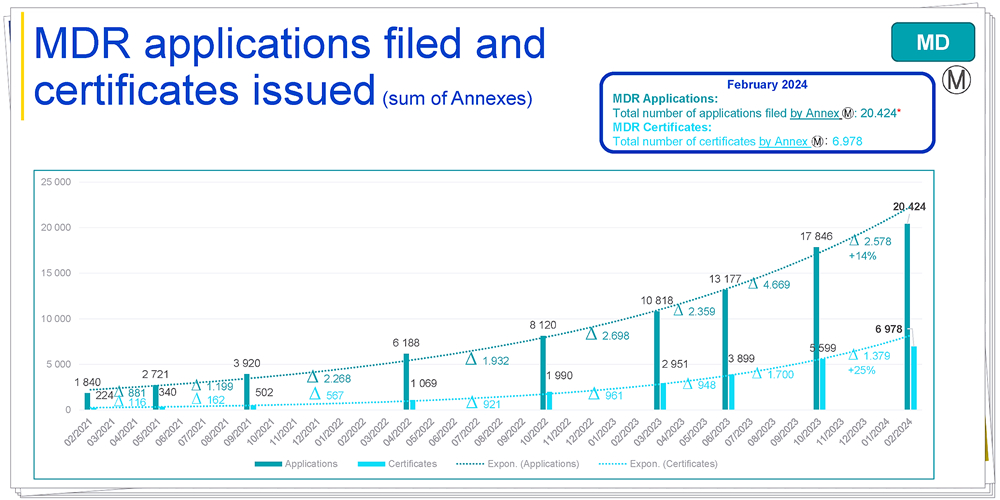
解读:已提交20424份MDR申请,已颁发6978份MDR证书,相比2023年10月:MDR申请增加2578份、增幅14%;MDR证书增加1379份、增幅25%。
2.MDR申请提交与签约数量的对比
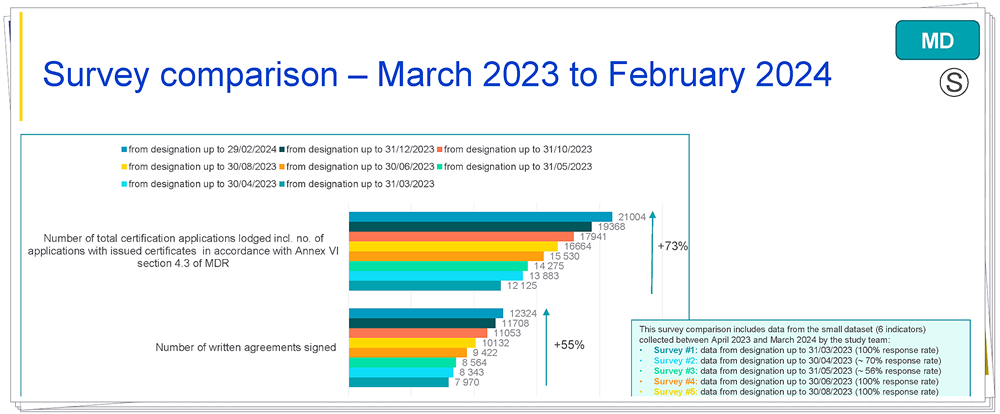
解读:与2023年3月相比,提交申请数量增长73%,书面协议签署数量增长55%。
3.MDR申请提交至签约的耗时
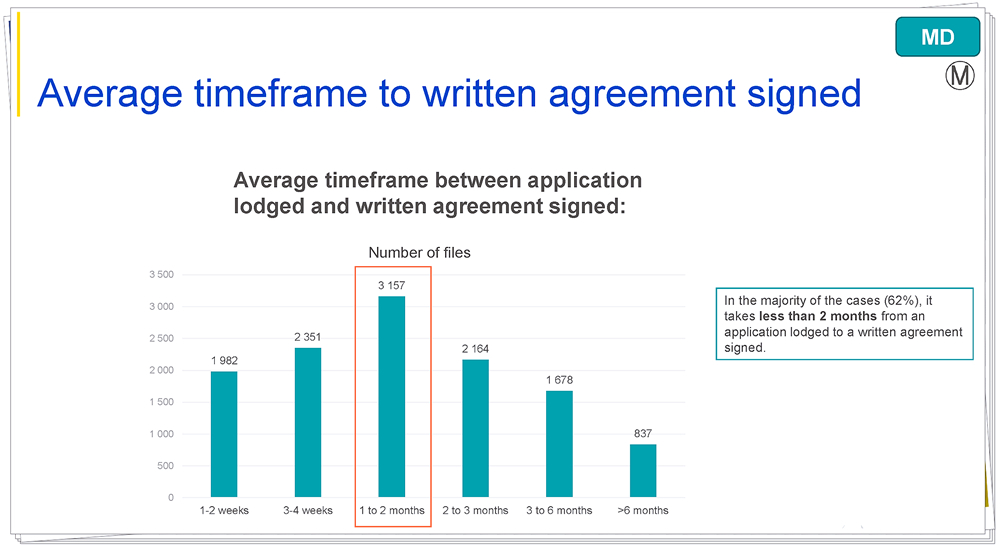
解读:从提交申请至签署书面协议的平均时间间隔为1-2个月,在占比62%的大多数情况下,从提交申请至签署书面协议需要少于2个月的时间。
4.MDR申请被拒绝的原因
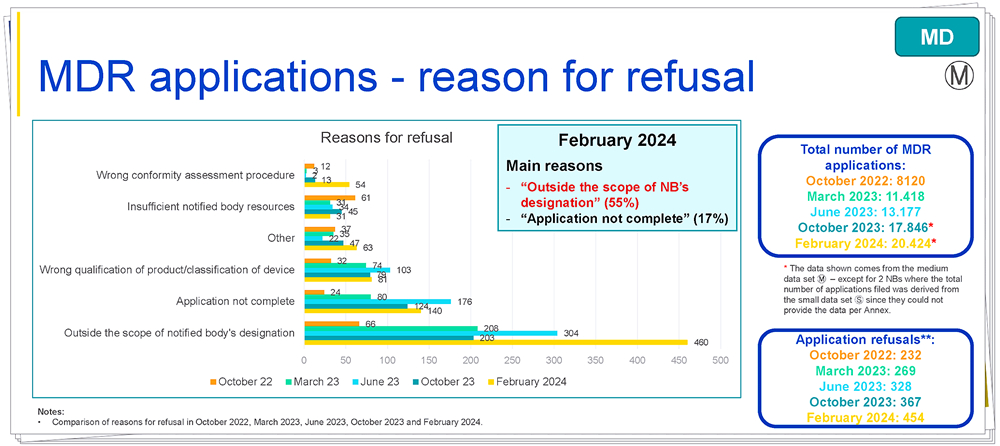
解读:共有454份申请被拒绝,被拒原因中占比最高(55%)为“不在公告机构的指定范围内”,其次为“申请不完整”(占比17%),之后占比由高到低依次为“错误的产品鉴定/设备分类”、“其他原因”、“错误的符合性评估程序”、“公告机构资源不足”。
5.MDR公告机构颁发新证书所需的时间
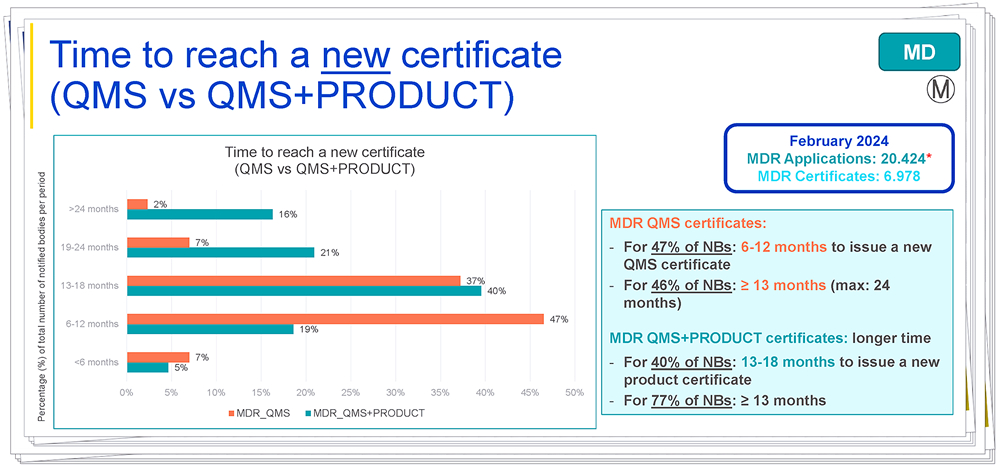
解读:公告机构颁发新证书(体系+产品)所需时间:
77%的公告机构:13个月及以上;
40%的公告机构:13-18个月;
21%:19-24个月;
19%:6-12个月;
16%:24个月及以上;
5%:少于6个月。
→ 欧盟CE证书办理,快·准·好的秘诀是什么?
√ 答案当然是久顺!始创于1996年,荷兰\英国\美国\中国均设公司,近30年全球合规技术专家,全程高效的欧盟合规服务:CE注册取证\技术文档编写\合规策略\体系辅导\上市后监督咨询\近20年资深欧代\临床方案设计和临床试验方案等。
MDR CE成功案例(篇幅有限,仅展示部分)↓
☑辅导3H(南京斯瑞奇)取得I类灭菌创口贴的CE-MDR证书;
☑助力海翔药业取得Is类灭菌CE-MDR证书;
☑助力台衡获I类测量CE-MDR证书;
☑辅导亚美斯特(天津)获得IIa类通气类产品的CE-MDR证书;
☑辅导杭州某生物企业成功通过Is类灭菌采样拭子的MDR体系审核(ISO13485);
☑助力深圳客户顺利通过IIa类敷料类产品的MDR体系审核(ISO13485);
☑辅导某跨国医疗器械企业取得IIb类监护类产品CE-MDR证书...